Installa l'app
How to install the app on iOS
Follow along with the video below to see how to install our site as a web app on your home screen.
Nota: This feature may not be available in some browsers.
Stai usando un browser molto obsoleto. Puoi incorrere in problemi di visualizzazione di questo e altri siti oltre che in problemi di sicurezza. .
Dovresti aggiornarlo oppure usare usarne uno alternativo, moderno e sicuro.
Dovresti aggiornarlo oppure usare usarne uno alternativo, moderno e sicuro.
CELL THER: SOLO GRAFICI, NEWS e FONDAMENTALI
-
 Trading Day 19 aprile Torino - Corso Gratuito sull'investimento
Trading Day 19 aprile Torino - Corso Gratuito sull'investimento

Migliora la tua strategia di trading con le preziose intuizioni dei nostri esperti su oro, materie prime, analisi tecnica, criptovalute e molto altro ancora. Iscriviti subito per partecipare gratuitamente allo Swissquote Trading Day.
Per continuare a leggere visita questo LINK
Più opzioni
Chi ha risposto?amedeo8
Corsi / Ricorsi
- Registrato
- 13/1/09
- Messaggi
- 16.465
- Punti reazioni
- 263
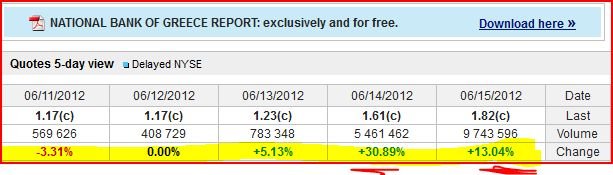
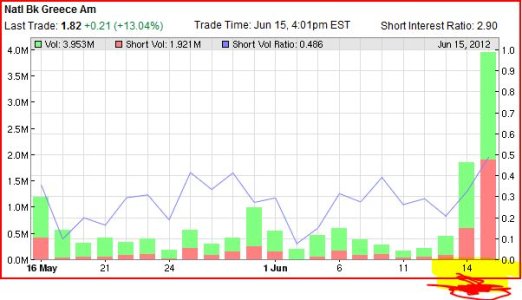
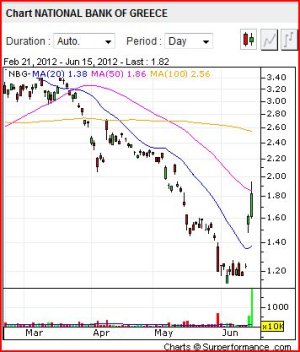
National Bank of Greece
da amnuale il rientro dallo short...........da martedì scorso.............
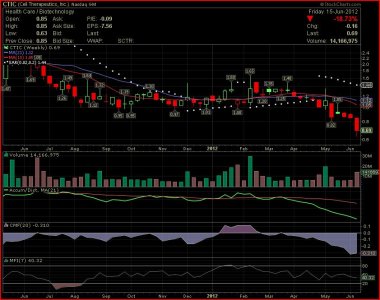
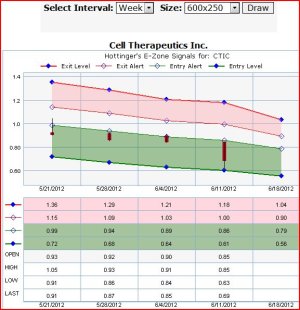
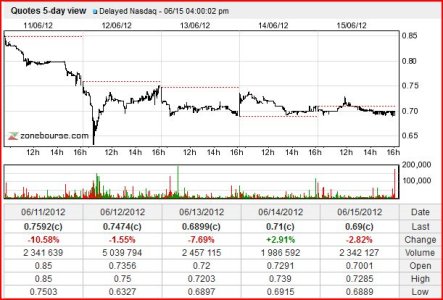
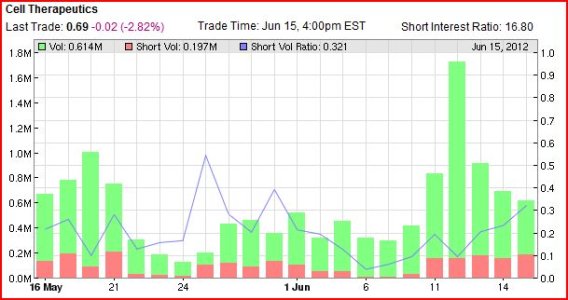
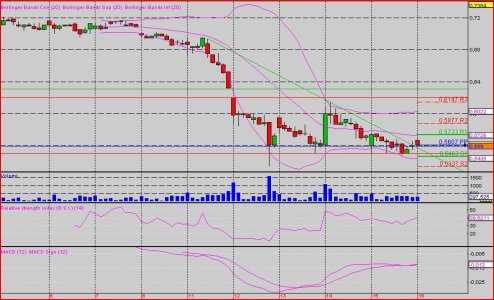
CTIC............ quando ci saranno notizie ........VERAMENTE price sensitive.........dovrebbe fare QUALCOSA DI SIMILE............
Vedi l'allegato 1607923
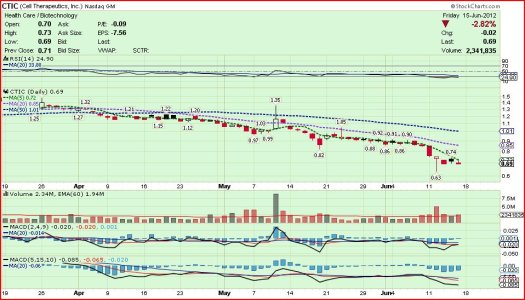
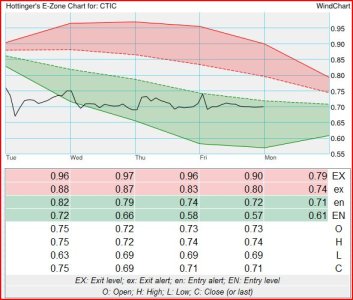
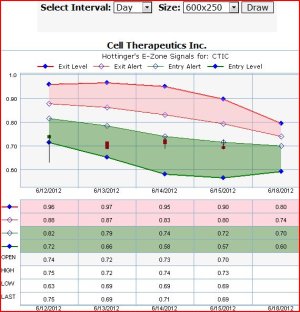
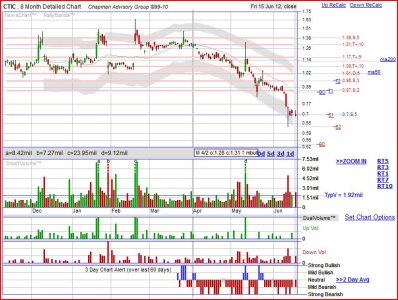
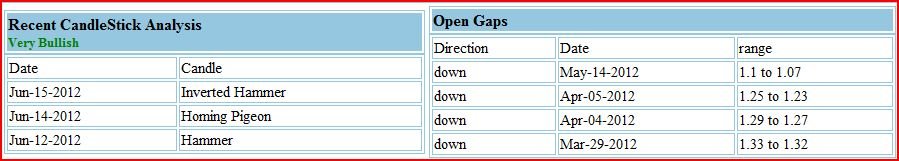
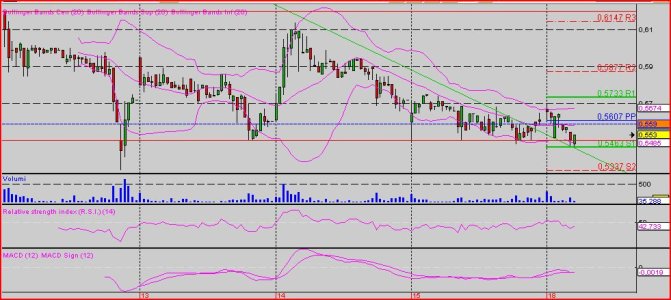
Vedi l'allegato 1607924 Vedi l'allegato 1607925
e quali sarebbero??? per me solo la dipartita di jb sarà una notizia price sensitive anzi molto price sensitive e farà fare al titolo uno scatto epocaleee come mai si è visto sulla faccia della terra!
amedeo8
Corsi / Ricorsi
- Registrato
- 13/1/09
- Messaggi
- 16.465
- Punti reazioni
- 263
amedeo8
Corsi / Ricorsi
- Registrato
- 13/1/09
- Messaggi
- 16.465
- Punti reazioni
- 263
CELL THERAPEUTICS: INIZIATA L'ISCRIZIONE ALLO STUDIO SU TOSEDOSTAT
AGI.it .............08:59 18 GIU 2012
Cell Therapeutics, Inc. ("CTI") (NASDAQ e MTA: CTIC) ha annunciato oggi che l'Universita' di Washington ("UW") ha iniziato ad arruolare pazienti in unaa'sperimentazione di fase II randomizzata che ha lo scopo di valutare la combinazione di tosedostat con citarabina o decitabina in pazienti anziani affetti da leucemia mieloide acutaa'("LMA") o sindrome mielodisplastica ("SMD") ad alto rischio di nuova diagnosi.Lo studio e' condotto dai Dott.ri John Pagel e Elihu Estey, della Scuola di Medicina dellaa'University of Washington e del Fred Hutchinson Cancer Research Center."Si tratta del primo studio in cui si esaminano gli effetti di tosedostat in combinazione con ditarabina o con decitabina come terapia di prima linea. Lo studio valutera' il modo in cui i pazienti tollerano queste combinazioni e la loro efficacia. Dato che non esistono progressi importanti nel trattamento dei pazienti anziani con LMA e che i risultati di uno studioprecedente sullo stesso tosedostat in pazienti recidivanti o refrattari con LMA o SMD hannoa'mostrato dei promettenti effetti anti-leucemici e una tollerabilita' accettabile, speriamo che questo studio dimostrera' che tosedostat aumenta la limitata efficacia di questi agenti antileucemici di uso comune" ha dichiarato il Dott. Estey.Gli obiettivi primari dello studio sono la determinazione dei tassi di sopravvivenza e di rispostaa'completa ("CR") a quattro mesi di tosedostat in combinazione con citarabina o decitabina nellaa'LMA non trattata o SMD ad alto rischio. Gli obiettivi secondari sono la valutazione dellaa'sicurezza e dell'efficacia di tosedostat in combinazione con citarabina o decitabina, la determinazione del tasso di mortalita' correlato al trattamento (definito come decesso entro ia'primi 30 giorni dall'inizio del trattamento) e la stima dei tassi di sopravvivenza libera da malattia, sopravvivenza a un anno e sopravvivenza globale.a' .
AGI.it .............08:59 18 GIU 2012
Cell Therapeutics, Inc. ("CTI") (NASDAQ e MTA: CTIC) ha annunciato oggi che l'Universita' di Washington ("UW") ha iniziato ad arruolare pazienti in unaa'sperimentazione di fase II randomizzata che ha lo scopo di valutare la combinazione di tosedostat con citarabina o decitabina in pazienti anziani affetti da leucemia mieloide acutaa'("LMA") o sindrome mielodisplastica ("SMD") ad alto rischio di nuova diagnosi.Lo studio e' condotto dai Dott.ri John Pagel e Elihu Estey, della Scuola di Medicina dellaa'University of Washington e del Fred Hutchinson Cancer Research Center."Si tratta del primo studio in cui si esaminano gli effetti di tosedostat in combinazione con ditarabina o con decitabina come terapia di prima linea. Lo studio valutera' il modo in cui i pazienti tollerano queste combinazioni e la loro efficacia. Dato che non esistono progressi importanti nel trattamento dei pazienti anziani con LMA e che i risultati di uno studioprecedente sullo stesso tosedostat in pazienti recidivanti o refrattari con LMA o SMD hannoa'mostrato dei promettenti effetti anti-leucemici e una tollerabilita' accettabile, speriamo che questo studio dimostrera' che tosedostat aumenta la limitata efficacia di questi agenti antileucemici di uso comune" ha dichiarato il Dott. Estey.Gli obiettivi primari dello studio sono la determinazione dei tassi di sopravvivenza e di rispostaa'completa ("CR") a quattro mesi di tosedostat in combinazione con citarabina o decitabina nellaa'LMA non trattata o SMD ad alto rischio. Gli obiettivi secondari sono la valutazione dellaa'sicurezza e dell'efficacia di tosedostat in combinazione con citarabina o decitabina, la determinazione del tasso di mortalita' correlato al trattamento (definito come decesso entro ia'primi 30 giorni dall'inizio del trattamento) e la stima dei tassi di sopravvivenza libera da malattia, sopravvivenza a un anno e sopravvivenza globale.a' .
CELL THERAPEUTICS: INIZIATA L'ISCRIZIONE ALLO STUDIO SU TOSEDOSTAT
AGI.it .............08:59 18 GIU 2012
Cell Therapeutics, Inc. ("CTI") (NASDAQ e MTA: CTIC) ha annunciato oggi che l'Universita' di Washington ("UW") ha iniziato ad arruolare pazienti in unaa'sperimentazione di fase II randomizzata che ha lo scopo di valutare la combinazione di tosedostat con citarabina o decitabina in pazienti anziani affetti da leucemia mieloide acutaa'("LMA") o sindrome mielodisplastica ("SMD") ad alto rischio di nuova diagnosi.Lo studio e' condotto dai Dott.ri John Pagel e Elihu Estey, della Scuola di Medicina dellaa'University of Washington e del Fred Hutchinson Cancer Research Center."Si tratta del primo studio in cui si esaminano gli effetti di tosedostat in combinazione con ditarabina o con decitabina come terapia di prima linea. Lo studio valutera' il modo in cui i pazienti tollerano queste combinazioni e la loro efficacia. Dato che non esistono progressi importanti nel trattamento dei pazienti anziani con LMA e che i risultati di uno studioprecedente sullo stesso tosedostat in pazienti recidivanti o refrattari con LMA o SMD hannoa'mostrato dei promettenti effetti anti-leucemici e una tollerabilita' accettabile, speriamo che questo studio dimostrera' che tosedostat aumenta la limitata efficacia di questi agenti antileucemici di uso comune" ha dichiarato il Dott. Estey.Gli obiettivi primari dello studio sono la determinazione dei tassi di sopravvivenza e di rispostaa'completa ("CR") a quattro mesi di tosedostat in combinazione con citarabina o decitabina nellaa'LMA non trattata o SMD ad alto rischio. Gli obiettivi secondari sono la valutazione dellaa'sicurezza e dell'efficacia di tosedostat in combinazione con citarabina o decitabina, la determinazione del tasso di mortalita' correlato al trattamento (definito come decesso entro ia'primi 30 giorni dall'inizio del trattamento) e la stima dei tassi di sopravvivenza libera da malattia, sopravvivenza a un anno e sopravvivenza globale.a' .
Elihu Estey, MD
Dr. Estey is an expert in treatment of acute myeloid leukemia (AML) and myelodysplastic syndromes (MDS). He serves as an advisor to the Food and Drug Administration regarding new drugs in AML
•Professor, Division of Hematology, University of Washington School of Medicine
•Member, Fred Hutchinson Cancer Research Center
John M. Pagel, MD, PhD
Title
•Associate Member, Clinical Research Division, Fred Hutchinson Cancer Research Center
•Associate Professor, Medical Oncology Division, University of Washington School of Medicine
Clinical Expertise
•Lymphomas, including Hodgkin's lymphoma and non-Hodgkin's lymphoma
•Acute leukemia
•Chronic leukemia
•Transplantation
•Novel targeted therapies
•Radiolabeled antibody therapies
His current research explores innovative approaches to delivering targeted radiation to cancer cells; ways to better treat patients with acute myeloid leukemia (AML), lymphoma, and chronic lymphocytic leukemia (CLL); and, strategies that use the immune system to boost standard treatment.
Fiber
Sospeso allo Staf
- Registrato
- 30/6/06
- Messaggi
- 57.399
- Punti reazioni
- 1.234
CELL THERAPEUTICS: INIZIATA L'ISCRIZIONE ALLO STUDIO SU TOSEDOSTAT
AGI.it .............08:59 18 GIU 2012
Cell Therapeutics, Inc. ("CTI") (NASDAQ e MTA: CTIC) ha annunciato oggi che l'Universita' di Washington ("UW") ha iniziato ad arruolare pazienti in unaa'sperimentazione di fase II randomizzata che ha lo scopo di valutare la combinazione di tosedostat con citarabina o decitabina in pazienti anziani affetti da leucemia mieloide acutaa'("LMA") o sindrome mielodisplastica ("SMD") ad alto rischio di nuova diagnosi.Lo studio e' condotto dai Dott.ri John Pagel e Elihu Estey, della Scuola di Medicina dellaa'University of Washington e del Fred Hutchinson Cancer Research Center."Si tratta del primo studio in cui si esaminano gli effetti di tosedostat in combinazione con ditarabina o con decitabina come terapia di prima linea. Lo studio valutera' il modo in cui i pazienti tollerano queste combinazioni e la loro efficacia. Dato che non esistono progressi importanti nel trattamento dei pazienti anziani con LMA e che i risultati di uno studioprecedente sullo stesso tosedostat in pazienti recidivanti o refrattari con LMA o SMD hannoa'mostrato dei promettenti effetti anti-leucemici e una tollerabilita' accettabile, speriamo che questo studio dimostrera' che tosedostat aumenta la limitata efficacia di questi agenti antileucemici di uso comune" ha dichiarato il Dott. Estey.Gli obiettivi primari dello studio sono la determinazione dei tassi di sopravvivenza e di rispostaa'completa ("CR") a quattro mesi di tosedostat in combinazione con citarabina o decitabina nellaa'LMA non trattata o SMD ad alto rischio. Gli obiettivi secondari sono la valutazione dellaa'sicurezza e dell'efficacia di tosedostat in combinazione con citarabina o decitabina, la determinazione del tasso di mortalita' correlato al trattamento (definito come decesso entro ia'primi 30 giorni dall'inizio del trattamento) e la stima dei tassi di sopravvivenza libera da malattia, sopravvivenza a un anno e sopravvivenza globale.a' .
scusate ma questi di Cti non dovevano iniziare uno studio di fase III con Tosedostat dopo l'acquisto della licenza per venderlo in America da Chroma Therapeutics in marzo 2011?
questo studio di fase II è sponsorizzato ? chi lo paga?
qualcuno sa qualcosa?
scusate ma questi di Cti non dovevano iniziare uno studio di fase III con Tosedostat dopo l'acquisto della licenza per venderlo in America da Chroma Therapeutics in marzo 2011?
Ciao.
Non vorrei dire castronerie ma credo che lo studio dell'università sia indipendente come mi pare quello sul pixantrone per la sclerosi multipla e su opaxio per il glioblastoma.
Però potrei sbagliarmi.
scusate ma questi di Cti non dovevano iniziare uno studio di fase III con Tosedostat dopo l'acquisto della licenza per venderlo in America da Chroma Therapeutics in marzo 2011?
questo studio di fase II è sponsorizzato ? chi lo paga?
qualcuno sa qualcosa?
.................scusa mi sà che ho detto delle castronerie prima.
Comunque lo studio in fase 3 riguarderebbe pazienti con recidiva e refrattaria mentre questo riguarda una prima linea in combinazione.
Comunque notizia positiva.
Ciao.
amedeo8
Corsi / Ricorsi
- Registrato
- 13/1/09
- Messaggi
- 16.465
- Punti reazioni
- 263
scusate ma questi di Cti non dovevano iniziare uno studio di fase III con Tosedostat dopo l'acquisto della licenza per venderlo in America da Chroma Therapeutics in marzo 2011?
questo studio di fase II è sponsorizzato ? chi lo paga?
qualcuno sa qualcosa?
https://www.google.it/search?q=afte...&rls=org.mozilla:it:official&client=firefox-a
Nel calendario delle consultazioni FDA, il 20 giugno c'è questo: Oncologic Drugs Advisory Committee
Per tutto il mese di giungo è così programmato:
June 13 - Circulatory System Devices Panel of the Medical Devices Advisory Committee
June 20 - Oncologic Drugs Advisory Committee
June 21 - General and Plastic Surgery Devices Panel of the Medical Devices Advisory Committee
June 27-28 - Cancelled Cellular, Tissue and Gene Therapies Advisory Committee
June 27-28 - Orthopaedic and Rehabilitation Devices Panel of the Medical Devices Advisory Committee
June 28-29 - Risk Communication Advisory Committee
Frugate nel sito ufficiale della FDA:
Advisory Committee Calendar
U S Food and Drug Administration Home Page
Oppure qui:
FDA Calendar | Trading Strategies For Forex And Stock Market Day Trader
finanzanostop.borse.it/calendar/#action=ai1ec_mont...ai1ec_month_offset=1
Per quanto riguarda Cell non è oggetto di consultazione nei mesi a venire, anche perchè, relativamente a Pix 301, come sappiamo, deve ripresentare la NDA. Riporto lo stralcio:
...l'unico modo per avere Pixuvri eventualmente in considerazione in una successiva riunione ODAC era per CTI di ritirarsi e poi ripresentare la NDA . CTI prevede di ripresentare la NDA nel 2012pharmabiz.com/NewsDetails.aspx?aid=67266&sid=2
Ctic, al momento, ritengo abbia spostato l'attenzione su altro. Deve programmare la fase III per Pacritinib e si deve concludere il finanziamento concordato con il Peizer (la Socius), di cui manca la seconda tranche. Inoltre, ha in programma la fase III per Tesodostat e deve commercializzare Pix 301 in Europa.
E' probabile che abbia scelto e potuto allargare gli interessi (Pacritinib e Tosedostat) perchè forte degli introiti che prevede dalla commercializzazione del Pix 301 in Europa.
Per questo, il mio focus (forse mi sbaglierò) è concentrato sulla definizione del finanziamento con la Socius e suppongo che le "mosse" successive verrano fatte proprio dopo la sistemazione di questo aspetto finanziario.
Per tutto il mese di giungo è così programmato:
June 13 - Circulatory System Devices Panel of the Medical Devices Advisory Committee
June 20 - Oncologic Drugs Advisory Committee
June 21 - General and Plastic Surgery Devices Panel of the Medical Devices Advisory Committee
June 27-28 - Cancelled Cellular, Tissue and Gene Therapies Advisory Committee
June 27-28 - Orthopaedic and Rehabilitation Devices Panel of the Medical Devices Advisory Committee
June 28-29 - Risk Communication Advisory Committee
Frugate nel sito ufficiale della FDA:
Advisory Committee Calendar
U S Food and Drug Administration Home Page
Oppure qui:
FDA Calendar | Trading Strategies For Forex And Stock Market Day Trader
finanzanostop.borse.it/calendar/#action=ai1ec_mont...ai1ec_month_offset=1
Per quanto riguarda Cell non è oggetto di consultazione nei mesi a venire, anche perchè, relativamente a Pix 301, come sappiamo, deve ripresentare la NDA. Riporto lo stralcio:
...l'unico modo per avere Pixuvri eventualmente in considerazione in una successiva riunione ODAC era per CTI di ritirarsi e poi ripresentare la NDA . CTI prevede di ripresentare la NDA nel 2012pharmabiz.com/NewsDetails.aspx?aid=67266&sid=2
Ctic, al momento, ritengo abbia spostato l'attenzione su altro. Deve programmare la fase III per Pacritinib e si deve concludere il finanziamento concordato con il Peizer (la Socius), di cui manca la seconda tranche. Inoltre, ha in programma la fase III per Tesodostat e deve commercializzare Pix 301 in Europa.
E' probabile che abbia scelto e potuto allargare gli interessi (Pacritinib e Tosedostat) perchè forte degli introiti che prevede dalla commercializzazione del Pix 301 in Europa.
Per questo, il mio focus (forse mi sbaglierò) è concentrato sulla definizione del finanziamento con la Socius e suppongo che le "mosse" successive verrano fatte proprio dopo la sistemazione di questo aspetto finanziario.
Cell Therapeutics si prepara al lancio commerciale di Pixuvri© nell'UE. Ilriallineamento delle risorse e delle priorità del suo portfolio riduce il burn rate di oltre il 30% Una ricerca di mercato conferma la possibilità che l'UE sia un mercato interessante per Pixuvri© Dare priorità alle risorse necessarie ad accelerare laprogressione di pacritinib verso la Fase III nel 4Q 2012 La nuova assegnazione delle priorità determinerà una riduzione di oltre il 30% del burn rate operativo Steven Benner M.D., M.H.S., nominato Chief Medical Officer alla guida dello sviluppo deifarmaci antineoplastici Seattle, 20 giugno 2012. Cell Therapeutics, Inc. ("CTI") (NASDAQ e MTA: CTIC), azienda impegnata a trasformare le conoscenze scientifiche in terapie antitumorali innovative, ha annunciato oggi il riallineamento delle sue risorse el'attribuzione di nuove priorità alla pipeline dei prodotti in sviluppo, al fine di concentrarsi sul lancio di Pixuvri nell'UE e di accelerare la progressione verso gli studi clinici di Fase III di pacritinib, l'inibitore JAK 2 altamente selettivo che CTI ha acquistato di recente. Di conseguenza, i costi di esercizio di CTI si ridurranno da una media di USD 6,5 milioni al mese a una media di USD 4,5 milioni al mese. "Una ricerca di mercato condotta nei cinque principali mercati dell'UE conferma unsignificativo interesse da parte dei medici per l'utilizzo del prodotto nella popolazione dei pazienti di riferimento. Alla luce delle significative vendite potenziali di Pixuvri©, della recente acquisizione di pacritinib e dell'interesse manifestatodagli sperimentatori per la partecipazione agli studi cardine sul prodotto, riteniamo che il modo migliore di impiegare le nostre limitate risorse per realizzare a breve termine valore per gli azionisti consista nel concentrare le risorse sul lancio diPixuvri e sull'accelerazione dell'avvio degli studi di Fase III su pacritinib", ha commentato James A. Bianco, M.D., Chief Executive Officer di CTI.
3101 Western Ave. #600 Seattle, WA 98121
T 206.282.7100 F 206.284.6206
Pagina 2 di 5
"Stiamo procedendo a una nuova valutazione del disegno di studio clinico di Fase III di tostedostat, prendendo in considerazione gli studi tanto nei soggetti refrattari quanto nel trattamento di prima linea" ha aggiunto Steven E. Benner, M.D., M.H.S, CMOdi CTI. "Due studi in corso di Fase II, sponsorizzati dagli sperimentatori, stanno esaminando l'attività della combinazione di tosedostat con gli agenti ipometilanti (HMA); dovremmo quindi, entro l'inizio del prossimo anno, avere dati a sufficienza perprendere una decisione basata sull'evidenza circa il disegno dello studio che consenta una buona riuscita in termini regolatori e commerciali." Pixuvri (pixantrone) Pixuvri è un nuovo aza-antrecenedione con proprietà strutturali e fisico-chimiche uniche.Diversamente da altri composti correlati, Pixuvri forma addotti stabili con il DNA e nei modelli preclinici presenta un'attività anti-linfoma superiore rispetto ai composti correlati. La struttura di Pixuvri è stato formulato in modo che non possa legareil ferro e perpetuare la produzione di radicali ossigeno o formare un metabolita idrossile di lunga durata, molecole che sono entrambe alla base dei meccanismi putativi della cardiotossicità acuta e cronica indotta dalle antracicline. Queste nuoveproprietà farmacologiche permettono a Pixuvri di essere somministrato ai pazienti con tempi di esposizione alle antracicline prossimi al massimo senza tassi inaccettabili di cardiotossicità e, dato che Pixuvri non è un vescicante, è possibilesomministrarlo in maniera sicura tramite catetere periferico intravenoso. A maggio 2012, Pixuvri ha ricevuto l'autorizzazione condizionata all'immissione in commercio nell'UE come monoterapia per il trattamento di pazienti adulti con LNH aggressivirecidivanti o refrattari multipli. Il beneficio del trattamento con Pixuvri non è stato stabilito per i pazienti quando viene utilizzato come chemioterapia di quinta linea o superiore in pazienti refrattari alla terapia precedente. Il riassunto dellecaratteristiche del prodotto ("RCP") include le informazioni complete sulla prescrizione, compreso il profilo di sicurezza ed efficacia di Pixuvri nell'indicazione approvata. Il riassunto delle caratteristiche del prodotto è disponibile all'indirizzohttp://ec.europa.eu/health/documents/community-register/html/h764.htm#ProcList. Attualmente CTI sta reclutando pazienti in uno studio di Fase III di confronto tra pixantrone + rituximab e gemcitabina + rituximab nel linfoma non Hodgkin aggressivo acellule B. La partecipazione dei centri europei allo studio è prevista nei prossimi mesi dell'anno. Al momento, Pixuvri è disponibile nell'UE tramite i programmi a carattere nominativo (Named Patient Programs). Pixuvri non è approvato per lacommercializzazione degli Stati Uniti.
3101 Western Ave. #600 Seattle, WA 98121
T 206.282.7100 F 206.284.6206
Pagina 3 di 5
Informazioni sull'autorizzazione condizionata all'immissione in commercio Analogamente alle normesull'approvazione accelerata vigenti negli Stati Uniti, le autorizzazioni condizionate all'immissione in commercio sono garantite per i medicinali accompagnati da una valutazione positiva del rapporto rischio/beneficio, che soddisfano esigenze medicheancora insoddisfatte e la cui disponibilità si tradurrebbe in un beneficio significativo per la salute pubblica. L'autorizzazione condizionata all'immissione in commercio è rinnovabile di anno in anno. Secondo le disposizioni dell'autorizzazionecondizionata all'immissione in commercio per Pixuvri, CTI dovrà completare uno studio post-marketing avente come fine la conferma del beneficio clinico precedentemente osservato. Il Comitato per i Medicinali per Uso Umano (CHMP) dell'Agenzia Europea per i Medicinali (EMA) ha accettato PIX306, la sperimentazione clinica in Fase III controllata randomizzata in corso di CTI, sul confronto fra Pixuvri-rituximab e gemcitabina-rituximab nei pazienti che hanno recidivato dopo uno fino a tre regimi precedenti per NHL aggressivo delle cellule B e che non sono eleggibili per il trapianto autologo di cellule staminali. Come condizione per l'approvazione, CTI ha concordato di avere a disposizione i risultati della sperimentazione clinica PIX306 entro giugno 2015.Pacritinib Pacritinib è un inibitore della tirosina chinasi (TKI), da assumere oralmente, una volta al giorno, con una duplice attività contro la JAK2V617F clonale e la tirosina chinasi 3 FMS simile (FLT3). È stato dimostrato che le mutazioni in questechinasi sono direttamente legate allo sviluppo di una varietà di tumori connessi al sangue, comprese la MPD, le leucemie e i linfomi. Pacritinib ha dimostrato risultati incoraggianti negli studi di Fase I e II per i pazienti affetti da mielofibrosi e, per questa malattia, è previsto uno studio di Fase III. FLT3 è un gene comunemente mutato che è stato trovato nei pazienti affetti da leucemia mieloide acuta ("AML") e le sue mutazioni attivanti hanno dimostrato essere un marcatore prognostico negativo perl'esito clinico suggerendo un possibile ruolo futuro per il trattamento della leucemia mieloide acuta. Tosedostat Tosedostat è un inibitore orale dell'aminopeptidasi che, nel corso di sperimentazioni cliniche di Fase I-II, ha evidenziato significativerisposte antitumorali nei confronti degli emotumori e dei tumori solidi. CTI esercita diritti esclusivi di marketing e cosviluppo per il Nord, Centro e Sud America su tosedostat, un farmaco candidato di Chroma Therapeutics Ltd. Cell Therapeutics, Inc. Con sede a Seattle, CTI è un'azienda biofarmaceutica impegnata nello sviluppo di un portafoglio integrato di prodotti oncologici mirati a rendere i tumori maggiormente trattabili. Per ulteriori informazioni visitare il sito http://www.celltherapeutics.com/.Per ricevere avvisi per e-mail e feed RSS, accedere al sito Web
3101 Western Ave. #600 Seattle, WA 98121
T 206.282.7100 F 206.284.6206
Pagina 2 di 5
"Stiamo procedendo a una nuova valutazione del disegno di studio clinico di Fase III di tostedostat, prendendo in considerazione gli studi tanto nei soggetti refrattari quanto nel trattamento di prima linea" ha aggiunto Steven E. Benner, M.D., M.H.S, CMOdi CTI. "Due studi in corso di Fase II, sponsorizzati dagli sperimentatori, stanno esaminando l'attività della combinazione di tosedostat con gli agenti ipometilanti (HMA); dovremmo quindi, entro l'inizio del prossimo anno, avere dati a sufficienza perprendere una decisione basata sull'evidenza circa il disegno dello studio che consenta una buona riuscita in termini regolatori e commerciali." Pixuvri (pixantrone) Pixuvri è un nuovo aza-antrecenedione con proprietà strutturali e fisico-chimiche uniche.Diversamente da altri composti correlati, Pixuvri forma addotti stabili con il DNA e nei modelli preclinici presenta un'attività anti-linfoma superiore rispetto ai composti correlati. La struttura di Pixuvri è stato formulato in modo che non possa legareil ferro e perpetuare la produzione di radicali ossigeno o formare un metabolita idrossile di lunga durata, molecole che sono entrambe alla base dei meccanismi putativi della cardiotossicità acuta e cronica indotta dalle antracicline. Queste nuoveproprietà farmacologiche permettono a Pixuvri di essere somministrato ai pazienti con tempi di esposizione alle antracicline prossimi al massimo senza tassi inaccettabili di cardiotossicità e, dato che Pixuvri non è un vescicante, è possibilesomministrarlo in maniera sicura tramite catetere periferico intravenoso. A maggio 2012, Pixuvri ha ricevuto l'autorizzazione condizionata all'immissione in commercio nell'UE come monoterapia per il trattamento di pazienti adulti con LNH aggressivirecidivanti o refrattari multipli. Il beneficio del trattamento con Pixuvri non è stato stabilito per i pazienti quando viene utilizzato come chemioterapia di quinta linea o superiore in pazienti refrattari alla terapia precedente. Il riassunto dellecaratteristiche del prodotto ("RCP") include le informazioni complete sulla prescrizione, compreso il profilo di sicurezza ed efficacia di Pixuvri nell'indicazione approvata. Il riassunto delle caratteristiche del prodotto è disponibile all'indirizzohttp://ec.europa.eu/health/documents/community-register/html/h764.htm#ProcList. Attualmente CTI sta reclutando pazienti in uno studio di Fase III di confronto tra pixantrone + rituximab e gemcitabina + rituximab nel linfoma non Hodgkin aggressivo acellule B. La partecipazione dei centri europei allo studio è prevista nei prossimi mesi dell'anno. Al momento, Pixuvri è disponibile nell'UE tramite i programmi a carattere nominativo (Named Patient Programs). Pixuvri non è approvato per lacommercializzazione degli Stati Uniti.
3101 Western Ave. #600 Seattle, WA 98121
T 206.282.7100 F 206.284.6206
Pagina 3 di 5
Informazioni sull'autorizzazione condizionata all'immissione in commercio Analogamente alle normesull'approvazione accelerata vigenti negli Stati Uniti, le autorizzazioni condizionate all'immissione in commercio sono garantite per i medicinali accompagnati da una valutazione positiva del rapporto rischio/beneficio, che soddisfano esigenze medicheancora insoddisfatte e la cui disponibilità si tradurrebbe in un beneficio significativo per la salute pubblica. L'autorizzazione condizionata all'immissione in commercio è rinnovabile di anno in anno. Secondo le disposizioni dell'autorizzazionecondizionata all'immissione in commercio per Pixuvri, CTI dovrà completare uno studio post-marketing avente come fine la conferma del beneficio clinico precedentemente osservato. Il Comitato per i Medicinali per Uso Umano (CHMP) dell'Agenzia Europea per i Medicinali (EMA) ha accettato PIX306, la sperimentazione clinica in Fase III controllata randomizzata in corso di CTI, sul confronto fra Pixuvri-rituximab e gemcitabina-rituximab nei pazienti che hanno recidivato dopo uno fino a tre regimi precedenti per NHL aggressivo delle cellule B e che non sono eleggibili per il trapianto autologo di cellule staminali. Come condizione per l'approvazione, CTI ha concordato di avere a disposizione i risultati della sperimentazione clinica PIX306 entro giugno 2015.Pacritinib Pacritinib è un inibitore della tirosina chinasi (TKI), da assumere oralmente, una volta al giorno, con una duplice attività contro la JAK2V617F clonale e la tirosina chinasi 3 FMS simile (FLT3). È stato dimostrato che le mutazioni in questechinasi sono direttamente legate allo sviluppo di una varietà di tumori connessi al sangue, comprese la MPD, le leucemie e i linfomi. Pacritinib ha dimostrato risultati incoraggianti negli studi di Fase I e II per i pazienti affetti da mielofibrosi e, per questa malattia, è previsto uno studio di Fase III. FLT3 è un gene comunemente mutato che è stato trovato nei pazienti affetti da leucemia mieloide acuta ("AML") e le sue mutazioni attivanti hanno dimostrato essere un marcatore prognostico negativo perl'esito clinico suggerendo un possibile ruolo futuro per il trattamento della leucemia mieloide acuta. Tosedostat Tosedostat è un inibitore orale dell'aminopeptidasi che, nel corso di sperimentazioni cliniche di Fase I-II, ha evidenziato significativerisposte antitumorali nei confronti degli emotumori e dei tumori solidi. CTI esercita diritti esclusivi di marketing e cosviluppo per il Nord, Centro e Sud America su tosedostat, un farmaco candidato di Chroma Therapeutics Ltd. Cell Therapeutics, Inc. Con sede a Seattle, CTI è un'azienda biofarmaceutica impegnata nello sviluppo di un portafoglio integrato di prodotti oncologici mirati a rendere i tumori maggiormente trattabili. Per ulteriori informazioni visitare il sito http://www.celltherapeutics.com/.Per ricevere avvisi per e-mail e feed RSS, accedere al sito Web
Cell Therapeutics si prepara al lancio commerciale di Pixuvri® nell’UE. Il riallineamento delle risorse e delle priorità del suo portfolio riduce il burn rate di oltre il 30%
Una ricerca di mercato conferma la possibilità che l’UE sia un mercato interessante per Pixuvri®
Dare priorità alle risorse necessarie ad accelerare la progressione di pacritinib verso la Fase III nel 4Q 2012
La nuova assegnazione delle priorità determinerà una riduzione di oltre il 30% del burn rate operativo
Steven Benner M.D., M.H.S., nominato Chief Medical Officer alla guida dello sviluppo dei farmaci antineoplastici
Seattle, 20 giugno 2012. Cell Therapeutics, Inc. ("CTI") (NASDAQ e MTA: CTIC), azienda impegnata a trasformare le conoscenze scientifiche in terapie antitumorali innovative, ha annunciato oggi il riallineamento delle sue risorse e l’attribuzione di nuove priorità alla pipeline dei prodotti in sviluppo, al fine di concentrarsi sul lancio di Pixuvri nell'UE e di accelerare la progressione verso gli studi clinici di Fase III di pacritinib, l’inibitore JAK 2 altamente selettivo che CTI ha acquistato di recente. Di conseguenza, i costi di esercizio di CTI si ridurranno da una media di USD 6,5 milioni al mese a una media di USD 4,5 milioni al mese.
“Una ricerca di mercato condotta nei cinque principali mercati dell’UE conferma un significativo interesse da parte dei medici per l’utilizzo del prodotto nella popolazione dei pazienti di riferimento. Alla luce delle significative vendite potenziali di Pixuvri®, della recente acquisizione di pacritinib e dell’interesse manifestato dagli sperimentatori per la partecipazione agli studi cardine sul prodotto, riteniamo che il modo migliore di impiegare le nostre limitate risorse per realizzare a breve termine valore per gli azionisti consista nel concentrare le risorse sul lancio di Pixuvri e sull’accelerazione dell’avvio degli studi di Fase III su pacritinib”, ha commentato James A. Bianco, M.D., Chief Executive Officer di CTI.
“Stiamo procedendo a una nuova valutazione del disegno di studio clinico di Fase III di tostedostat, prendendo in considerazione gli studi tanto nei soggetti refrattari quanto nel trattamento di prima linea” ha aggiunto Steven E. Benner, M.D., M.H.S, CMO di CTI. “Due studi in corso di Fase II, sponsorizzati dagli sperimentatori, stanno esaminando l’attività della combinazione di tosedostat con gli agenti ipometilanti (HMA); dovremmo quindi, entro l’inizio del prossimo anno, avere dati a sufficienza per prendere una decisione basata sull’evidenza circa il disegno dello studio che consenta una buona riuscita in termini regolatori e commerciali.”
Pixuvri (pixantrone)
Pixuvri è un nuovo aza-antrecenedione con proprietà strutturali e fisico-chimiche uniche. Diversamente da altri composti correlati, Pixuvri forma addotti stabili con il DNA e nei modelli preclinici presenta un’attività anti-linfoma superiore rispetto ai composti correlati. La struttura di Pixuvri è stato formulato in modo che non possa legare il ferro e perpetuare la produzione di radicali ossigeno o formare un metabolita idrossile di lunga durata, molecole che sono entrambe alla base dei meccanismi putativi della cardiotossicità acuta e cronica indotta dalle antracicline. Queste nuove proprietà farmacologiche permettono a Pixuvri di essere somministrato ai pazienti con tempi di esposizione alle antracicline prossimi al massimo senza tassi inaccettabili di cardiotossicità e, dato che Pixuvri non è un vescicante, è possibile somministrarlo in maniera sicura tramite catetere periferico intravenoso.
A maggio 2012, Pixuvri ha ricevuto l’autorizzazione condizionata all’immissione in commercio nell’UE come monoterapia per il trattamento di pazienti adulti con LNH aggressivi recidivanti o refrattari multipli. Il beneficio del trattamento con Pixuvri non è stato stabilito per i pazienti quando viene utilizzato come chemioterapia di quinta linea o superiore in pazienti refrattari alla terapia precedente. Il riassunto delle caratteristiche del prodotto (“RCP”) include le informazioni complete sulla prescrizione, compreso il profilo di sicurezza ed efficacia di Pixuvri nell’indicazione approvata. Il riassunto delle caratteristiche del prodotto è disponibile all’indirizzo
Community register of medicinal products for human use.
Attualmente CTI sta reclutando pazienti in uno studio di Fase III di confronto tra pixantrone + rituximab e gemcitabina + rituximab nel linfoma non Hodgkin aggressivo a cellule B. La partecipazione dei centri europei allo studio è prevista nei prossimi mesi dell’anno.
Al momento, Pixuvri è disponibile nell'UE tramite i programmi a carattere nominativo (Named Patient Programs).
Pixuvri non è approvato per la commercializzazione degli Stati Uniti.
Informazioni sull’autorizzazione condizionata all’immissione in commercio
Analogamente alle norme sull’approvazione accelerata vigenti negli Stati Uniti, le autorizzazioni condizionate all’immissione in commercio sono garantite per i medicinali accompagnati da una valutazione positiva del rapporto rischio/beneficio, che soddisfano esigenze mediche ancora insoddisfatte e la cui disponibilità si tradurrebbe in un beneficio significativo per la salute pubblica. L’autorizzazione condizionata all’immissione in commercio è rinnovabile di anno in anno. Secondo le disposizioni dell’autorizzazione condizionata all’immissione in commercio per Pixuvri, CTI dovrà completare uno studio post-marketing avente come fine la conferma del beneficio clinico precedentemente osservato.
Il Comitato per i Medicinali per Uso Umano (CHMP) dell’Agenzia Europea per i Medicinali (EMA) ha accettato PIX306, la sperimentazione clinica in Fase III controllata randomizzata in corso di CTI, sul confronto fra Pixuvri-rituximab e gemcitabina-rituximab nei pazienti che hanno recidivato dopo uno fino a tre regimi precedenti per NHL aggressivo delle cellule B e che non sono eleggibili per il trapianto autologo di cellule staminali.
Come condizione per l’approvazione, CTI ha concordato di avere a disposizione i risultati della sperimentazione clinica PIX306 entro giugno 2015.
Pacritinib
Pacritinib è un inibitore della tirosina chinasi (TKI), da assumere oralmente, una volta al giorno, con una duplice attività contro la JAK2V617F clonale e la tirosina chinasi 3 FMS simile (FLT3). È stato dimostrato che le mutazioni in queste chinasi sono direttamente legate allo sviluppo di una varietà di tumori connessi al sangue, comprese la MPD, le leucemie e i linfomi. Pacritinib ha dimostrato risultati incoraggianti negli studi di Fase I e II per i pazienti affetti da mielofibrosi e, per questa malattia, è previsto uno studio di Fase III.
FLT3 è un gene comunemente mutato che è stato trovato nei pazienti affetti da leucemia mieloide acuta ("AML") e le sue mutazioni attivanti hanno dimostrato essere un marcatore prognostico negativo per l'esito clinico suggerendo un possibile ruolo futuro per il trattamento della leucemia mieloide acuta.
Tosedostat
Tosedostat è un inibitore orale dell'aminopeptidasi che, nel corso di sperimentazioni cliniche di Fase I-II, ha evidenziato significative risposte antitumorali nei confronti degli emotumori e dei tumori solidi. CTI esercita diritti esclusivi di marketing e cosviluppo per il Nord, Centro e Sud America su tosedostat, un farmaco candidato di Chroma Therapeutics Ltd.
Cell Therapeutics, Inc.
Con sede a Seattle, CTI è un’azienda biofarmaceutica impegnata nello sviluppo di un portafoglio integrato di prodotti oncologici mirati a rendere i tumori maggiormente trattabili. Per ulteriori informazioni visitare il sito Cell Therapeutics (CTI) Cancer Therapies and Cancer Drug Development Home Page - Cell Therapeutics, Inc..
Per ricevere avvisi per e-mail e feed RSS, accedere al sito Web
Investors - Cell Therapeutics, Inc. - Email Alerts
Questo comunicato contiene previsioni future per loro natura soggette a rischi ed incertezze, che potrebbero avere effetti significativi e/o influenzare negativamente i risultati futuri ed il prezzo di contrattazione dei titoli CTI. Nello specifico, i rischi e le incertezze che possono influire sullo sviluppo di pixuvri, pacritinib o tosedostat includono i rischi associati agli sviluppi preclinici e clinici propri del settore biofarmaceutico in genere e di pixuvri, pacritinib o tosedostat in particolare, comprendenti in modo non limitativo, la potenziale incapacità di pixuvri di dimostrasi sicuro ed efficace nel trattamento del linfoma non di Hodgkin recidivato o refrattario e/o di altri tumori come determinato dall'ente statunitense Food and Drug Administration (l'"FDA"); il fatto che pixuvri possa non essere immediatamente disponibile per i pazienti nell'UE; la potenziale incapacità di CTI di commercializzare pixuvri nel modo pianificato; il possibiule mancato lancio da parte di CTI di Pixuvri nell'UE quest'anno; la capacità di CTI di completare entro il giugno 2015 o mai la sperimentazione clinica PIX306 di pixuvri-rituximab a confronto con gemcitabine-rituximab in pazienti recidivati dopo da 1 a 3 regimi precedenti contro l'LNH a cellule B aggressivo, inidonei al trapianto autologo di cellule staminali, come richiesto dall'EMA, o di mettere a disposizione tali risultati entro il giugno 2015 o mai; la capacità di CTI di completare uno studio post-marketing mirato a confermare i benefici clinici osservati nel corso della ricerca PIX301;il mancato rinnovo dell’autorizzazione condizionale all’immissione in commercio per Pixuviri; il mancato avviamento entro il quarto trimestre del 2012 degli studi di Fase III sul pacritinib; la mancata dimostrazione della sicurezza e dell'efficacia di pacritinib nei confronti della mielofibrosi ("MF") primaria e della MF secondaria ad altri neoplasmi mieloproliferativi ("MPN"); la potenziale incapacità di tosedostat di dimostrarsi sicuro ed efficace nel trattamento di pazienti anziani con AML recentemente diagnosticata o con sindrome mielosdisplasica ad alto rischio (compresa la sua somministrazione assieme a citarabina o decitabine), come determinato dall'FDA e/o dall'EMA; il potenziale insuccesso degli studi combinatori di tosedostat con agenti ipometilanti ai fini del trattamento di AML e/o di MDS; l'incapacità degli studi sul tosedostat di conseguire i lori obiettivi primari o secondari: la mancata approvazione di tosedostat dall'FDA e/o dall'EMA; l'incapacità di CTI di predire o garantire i tempi o la distribuzione geografica del reclutamento per le sperimentazioni cliniche o il numero totale di pazienti reclutati; l'incapacità del riallineamento delle risorse di CTI e della riprioritarizzazione della pipeline prodotti di ridurre le spese di gestione aziendali da USD 6,5 milioni al mese ad una media di USD 4,5 milioni al mese o di oltre il 30% o la mancata capacità di CTI di continuare a raccogliere ulteriori capitali per finanziare le proprie operazioni in genere; comprendendo senza limitazioni fattori competitivi, sviluppi tecnologici, costi di sviluppo, produzione e vendita di pixuvri ; ed i fattori di rischio elencati di volta in volta nei documenti depositati presso la Securities and Exchange Commission, compresi, senza limitazioni, le ultimissime presentazioni da parte di CTI dei moduli Form 10-K, 8-K e 10-Q. Fatto salvo quanto previsto dalla legge, CTI non intende aggiornare o variare le sue previsioni future come risultato di nuove informazioni o sviluppi.
###
In Europa
Elena Bellacicca
T: +39 02 89659700
E: EBellacicca@cti-lifesciences.com
Negli USA
Media:
Dan Eramian
T: +1 206.272.4343
C: +1 206.854.1200
E: media@ctiseattle.com
CTI Press Room - Resources for the Media - Cell Therapeutics, Inc.
Investitori:
Ed Bell
T: +1 206.272.4345
Lindsey Jesch Logan
T: +1 206.272.4347
F: +1 206.272.4434
E: invest@ctiseattle.com
Investors - Cell Therapeutics, Inc. - Investors
Informazioni mediche
T: 800.715.0944
E: info@askarm.com
Una ricerca di mercato conferma la possibilità che l’UE sia un mercato interessante per Pixuvri®
Dare priorità alle risorse necessarie ad accelerare la progressione di pacritinib verso la Fase III nel 4Q 2012
La nuova assegnazione delle priorità determinerà una riduzione di oltre il 30% del burn rate operativo
Steven Benner M.D., M.H.S., nominato Chief Medical Officer alla guida dello sviluppo dei farmaci antineoplastici
Seattle, 20 giugno 2012. Cell Therapeutics, Inc. ("CTI") (NASDAQ e MTA: CTIC), azienda impegnata a trasformare le conoscenze scientifiche in terapie antitumorali innovative, ha annunciato oggi il riallineamento delle sue risorse e l’attribuzione di nuove priorità alla pipeline dei prodotti in sviluppo, al fine di concentrarsi sul lancio di Pixuvri nell'UE e di accelerare la progressione verso gli studi clinici di Fase III di pacritinib, l’inibitore JAK 2 altamente selettivo che CTI ha acquistato di recente. Di conseguenza, i costi di esercizio di CTI si ridurranno da una media di USD 6,5 milioni al mese a una media di USD 4,5 milioni al mese.
“Una ricerca di mercato condotta nei cinque principali mercati dell’UE conferma un significativo interesse da parte dei medici per l’utilizzo del prodotto nella popolazione dei pazienti di riferimento. Alla luce delle significative vendite potenziali di Pixuvri®, della recente acquisizione di pacritinib e dell’interesse manifestato dagli sperimentatori per la partecipazione agli studi cardine sul prodotto, riteniamo che il modo migliore di impiegare le nostre limitate risorse per realizzare a breve termine valore per gli azionisti consista nel concentrare le risorse sul lancio di Pixuvri e sull’accelerazione dell’avvio degli studi di Fase III su pacritinib”, ha commentato James A. Bianco, M.D., Chief Executive Officer di CTI.
“Stiamo procedendo a una nuova valutazione del disegno di studio clinico di Fase III di tostedostat, prendendo in considerazione gli studi tanto nei soggetti refrattari quanto nel trattamento di prima linea” ha aggiunto Steven E. Benner, M.D., M.H.S, CMO di CTI. “Due studi in corso di Fase II, sponsorizzati dagli sperimentatori, stanno esaminando l’attività della combinazione di tosedostat con gli agenti ipometilanti (HMA); dovremmo quindi, entro l’inizio del prossimo anno, avere dati a sufficienza per prendere una decisione basata sull’evidenza circa il disegno dello studio che consenta una buona riuscita in termini regolatori e commerciali.”
Pixuvri (pixantrone)
Pixuvri è un nuovo aza-antrecenedione con proprietà strutturali e fisico-chimiche uniche. Diversamente da altri composti correlati, Pixuvri forma addotti stabili con il DNA e nei modelli preclinici presenta un’attività anti-linfoma superiore rispetto ai composti correlati. La struttura di Pixuvri è stato formulato in modo che non possa legare il ferro e perpetuare la produzione di radicali ossigeno o formare un metabolita idrossile di lunga durata, molecole che sono entrambe alla base dei meccanismi putativi della cardiotossicità acuta e cronica indotta dalle antracicline. Queste nuove proprietà farmacologiche permettono a Pixuvri di essere somministrato ai pazienti con tempi di esposizione alle antracicline prossimi al massimo senza tassi inaccettabili di cardiotossicità e, dato che Pixuvri non è un vescicante, è possibile somministrarlo in maniera sicura tramite catetere periferico intravenoso.
A maggio 2012, Pixuvri ha ricevuto l’autorizzazione condizionata all’immissione in commercio nell’UE come monoterapia per il trattamento di pazienti adulti con LNH aggressivi recidivanti o refrattari multipli. Il beneficio del trattamento con Pixuvri non è stato stabilito per i pazienti quando viene utilizzato come chemioterapia di quinta linea o superiore in pazienti refrattari alla terapia precedente. Il riassunto delle caratteristiche del prodotto (“RCP”) include le informazioni complete sulla prescrizione, compreso il profilo di sicurezza ed efficacia di Pixuvri nell’indicazione approvata. Il riassunto delle caratteristiche del prodotto è disponibile all’indirizzo
Community register of medicinal products for human use.
Attualmente CTI sta reclutando pazienti in uno studio di Fase III di confronto tra pixantrone + rituximab e gemcitabina + rituximab nel linfoma non Hodgkin aggressivo a cellule B. La partecipazione dei centri europei allo studio è prevista nei prossimi mesi dell’anno.
Al momento, Pixuvri è disponibile nell'UE tramite i programmi a carattere nominativo (Named Patient Programs).
Pixuvri non è approvato per la commercializzazione degli Stati Uniti.
Informazioni sull’autorizzazione condizionata all’immissione in commercio
Analogamente alle norme sull’approvazione accelerata vigenti negli Stati Uniti, le autorizzazioni condizionate all’immissione in commercio sono garantite per i medicinali accompagnati da una valutazione positiva del rapporto rischio/beneficio, che soddisfano esigenze mediche ancora insoddisfatte e la cui disponibilità si tradurrebbe in un beneficio significativo per la salute pubblica. L’autorizzazione condizionata all’immissione in commercio è rinnovabile di anno in anno. Secondo le disposizioni dell’autorizzazione condizionata all’immissione in commercio per Pixuvri, CTI dovrà completare uno studio post-marketing avente come fine la conferma del beneficio clinico precedentemente osservato.
Il Comitato per i Medicinali per Uso Umano (CHMP) dell’Agenzia Europea per i Medicinali (EMA) ha accettato PIX306, la sperimentazione clinica in Fase III controllata randomizzata in corso di CTI, sul confronto fra Pixuvri-rituximab e gemcitabina-rituximab nei pazienti che hanno recidivato dopo uno fino a tre regimi precedenti per NHL aggressivo delle cellule B e che non sono eleggibili per il trapianto autologo di cellule staminali.
Come condizione per l’approvazione, CTI ha concordato di avere a disposizione i risultati della sperimentazione clinica PIX306 entro giugno 2015.
Pacritinib
Pacritinib è un inibitore della tirosina chinasi (TKI), da assumere oralmente, una volta al giorno, con una duplice attività contro la JAK2V617F clonale e la tirosina chinasi 3 FMS simile (FLT3). È stato dimostrato che le mutazioni in queste chinasi sono direttamente legate allo sviluppo di una varietà di tumori connessi al sangue, comprese la MPD, le leucemie e i linfomi. Pacritinib ha dimostrato risultati incoraggianti negli studi di Fase I e II per i pazienti affetti da mielofibrosi e, per questa malattia, è previsto uno studio di Fase III.
FLT3 è un gene comunemente mutato che è stato trovato nei pazienti affetti da leucemia mieloide acuta ("AML") e le sue mutazioni attivanti hanno dimostrato essere un marcatore prognostico negativo per l'esito clinico suggerendo un possibile ruolo futuro per il trattamento della leucemia mieloide acuta.
Tosedostat
Tosedostat è un inibitore orale dell'aminopeptidasi che, nel corso di sperimentazioni cliniche di Fase I-II, ha evidenziato significative risposte antitumorali nei confronti degli emotumori e dei tumori solidi. CTI esercita diritti esclusivi di marketing e cosviluppo per il Nord, Centro e Sud America su tosedostat, un farmaco candidato di Chroma Therapeutics Ltd.
Cell Therapeutics, Inc.
Con sede a Seattle, CTI è un’azienda biofarmaceutica impegnata nello sviluppo di un portafoglio integrato di prodotti oncologici mirati a rendere i tumori maggiormente trattabili. Per ulteriori informazioni visitare il sito Cell Therapeutics (CTI) Cancer Therapies and Cancer Drug Development Home Page - Cell Therapeutics, Inc..
Per ricevere avvisi per e-mail e feed RSS, accedere al sito Web
Investors - Cell Therapeutics, Inc. - Email Alerts
Questo comunicato contiene previsioni future per loro natura soggette a rischi ed incertezze, che potrebbero avere effetti significativi e/o influenzare negativamente i risultati futuri ed il prezzo di contrattazione dei titoli CTI. Nello specifico, i rischi e le incertezze che possono influire sullo sviluppo di pixuvri, pacritinib o tosedostat includono i rischi associati agli sviluppi preclinici e clinici propri del settore biofarmaceutico in genere e di pixuvri, pacritinib o tosedostat in particolare, comprendenti in modo non limitativo, la potenziale incapacità di pixuvri di dimostrasi sicuro ed efficace nel trattamento del linfoma non di Hodgkin recidivato o refrattario e/o di altri tumori come determinato dall'ente statunitense Food and Drug Administration (l'"FDA"); il fatto che pixuvri possa non essere immediatamente disponibile per i pazienti nell'UE; la potenziale incapacità di CTI di commercializzare pixuvri nel modo pianificato; il possibiule mancato lancio da parte di CTI di Pixuvri nell'UE quest'anno; la capacità di CTI di completare entro il giugno 2015 o mai la sperimentazione clinica PIX306 di pixuvri-rituximab a confronto con gemcitabine-rituximab in pazienti recidivati dopo da 1 a 3 regimi precedenti contro l'LNH a cellule B aggressivo, inidonei al trapianto autologo di cellule staminali, come richiesto dall'EMA, o di mettere a disposizione tali risultati entro il giugno 2015 o mai; la capacità di CTI di completare uno studio post-marketing mirato a confermare i benefici clinici osservati nel corso della ricerca PIX301;il mancato rinnovo dell’autorizzazione condizionale all’immissione in commercio per Pixuviri; il mancato avviamento entro il quarto trimestre del 2012 degli studi di Fase III sul pacritinib; la mancata dimostrazione della sicurezza e dell'efficacia di pacritinib nei confronti della mielofibrosi ("MF") primaria e della MF secondaria ad altri neoplasmi mieloproliferativi ("MPN"); la potenziale incapacità di tosedostat di dimostrarsi sicuro ed efficace nel trattamento di pazienti anziani con AML recentemente diagnosticata o con sindrome mielosdisplasica ad alto rischio (compresa la sua somministrazione assieme a citarabina o decitabine), come determinato dall'FDA e/o dall'EMA; il potenziale insuccesso degli studi combinatori di tosedostat con agenti ipometilanti ai fini del trattamento di AML e/o di MDS; l'incapacità degli studi sul tosedostat di conseguire i lori obiettivi primari o secondari: la mancata approvazione di tosedostat dall'FDA e/o dall'EMA; l'incapacità di CTI di predire o garantire i tempi o la distribuzione geografica del reclutamento per le sperimentazioni cliniche o il numero totale di pazienti reclutati; l'incapacità del riallineamento delle risorse di CTI e della riprioritarizzazione della pipeline prodotti di ridurre le spese di gestione aziendali da USD 6,5 milioni al mese ad una media di USD 4,5 milioni al mese o di oltre il 30% o la mancata capacità di CTI di continuare a raccogliere ulteriori capitali per finanziare le proprie operazioni in genere; comprendendo senza limitazioni fattori competitivi, sviluppi tecnologici, costi di sviluppo, produzione e vendita di pixuvri ; ed i fattori di rischio elencati di volta in volta nei documenti depositati presso la Securities and Exchange Commission, compresi, senza limitazioni, le ultimissime presentazioni da parte di CTI dei moduli Form 10-K, 8-K e 10-Q. Fatto salvo quanto previsto dalla legge, CTI non intende aggiornare o variare le sue previsioni future come risultato di nuove informazioni o sviluppi.
###
In Europa
Elena Bellacicca
T: +39 02 89659700
E: EBellacicca@cti-lifesciences.com
Negli USA
Media:
Dan Eramian
T: +1 206.272.4343
C: +1 206.854.1200
E: media@ctiseattle.com
CTI Press Room - Resources for the Media - Cell Therapeutics, Inc.
Investitori:
Ed Bell
T: +1 206.272.4345
Lindsey Jesch Logan
T: +1 206.272.4347
F: +1 206.272.4434
E: invest@ctiseattle.com
Investors - Cell Therapeutics, Inc. - Investors
Informazioni mediche
T: 800.715.0944
E: info@askarm.com